De 5. Juli huet Novo Nordisk e Phase III klineschen Test vun der CagriSema Injektioun a China gestart, den Zweck vun deem ass d'Sécherheet an d'Effizienz vun der CagriSema Injektioun mat Semeglutid bei fettleibeg an Iwwergewiicht Patienten a China ze vergläichen.
CagriSema Injektioun ass eng laangwierkend Kombinatiounstherapie ënner Entwécklung vum Novo Nordisk, d'Haaptkomponente si GLP-1 (glukagonähnlech Peptid-1) Rezeptor Agonist Smeglutid an e laangwierkend Amylin Analog Cagrilintid.CagriSema Injektioun kann subkutan eemol d'Woch verwalt ginn.
D'Haaptziel war CagriSema (2,4 mg/2,4 mg) mat Semeglutid oder Placebo eemol d'Woch subkutan ze vergläichen.Novo Nordisk huet d'Resultater vun engem Test vu CagriSema fir d'Behandlung vun der Stuf 2 Diabetis ugekënnegt, wat bewisen huet datt den hypoglycemesche Effekt vum CagriSema besser ass wéi dee vu Semeglutid, a bal 90% vun de Sujeten hunn den HbA1c Zil erreecht.
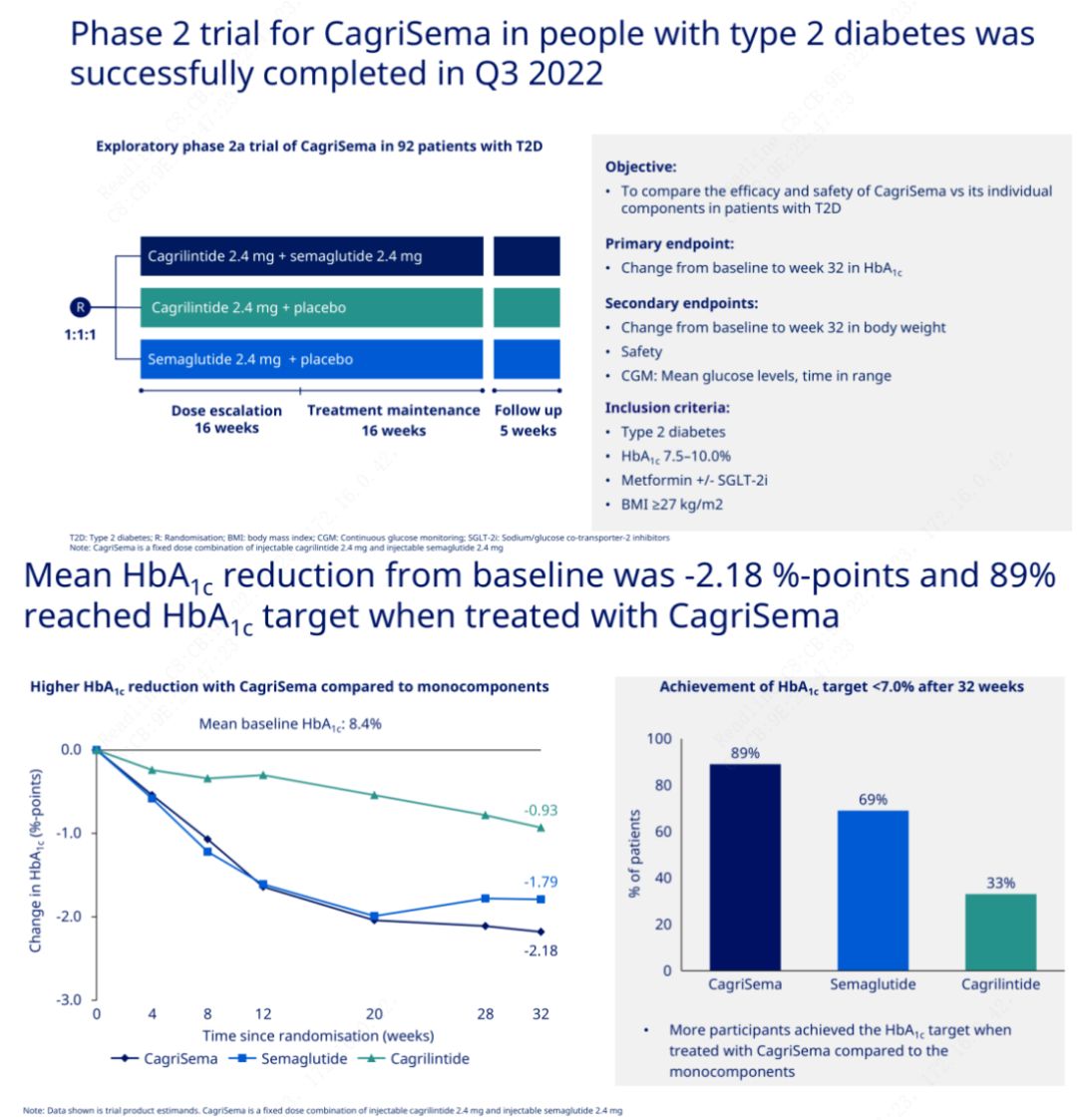
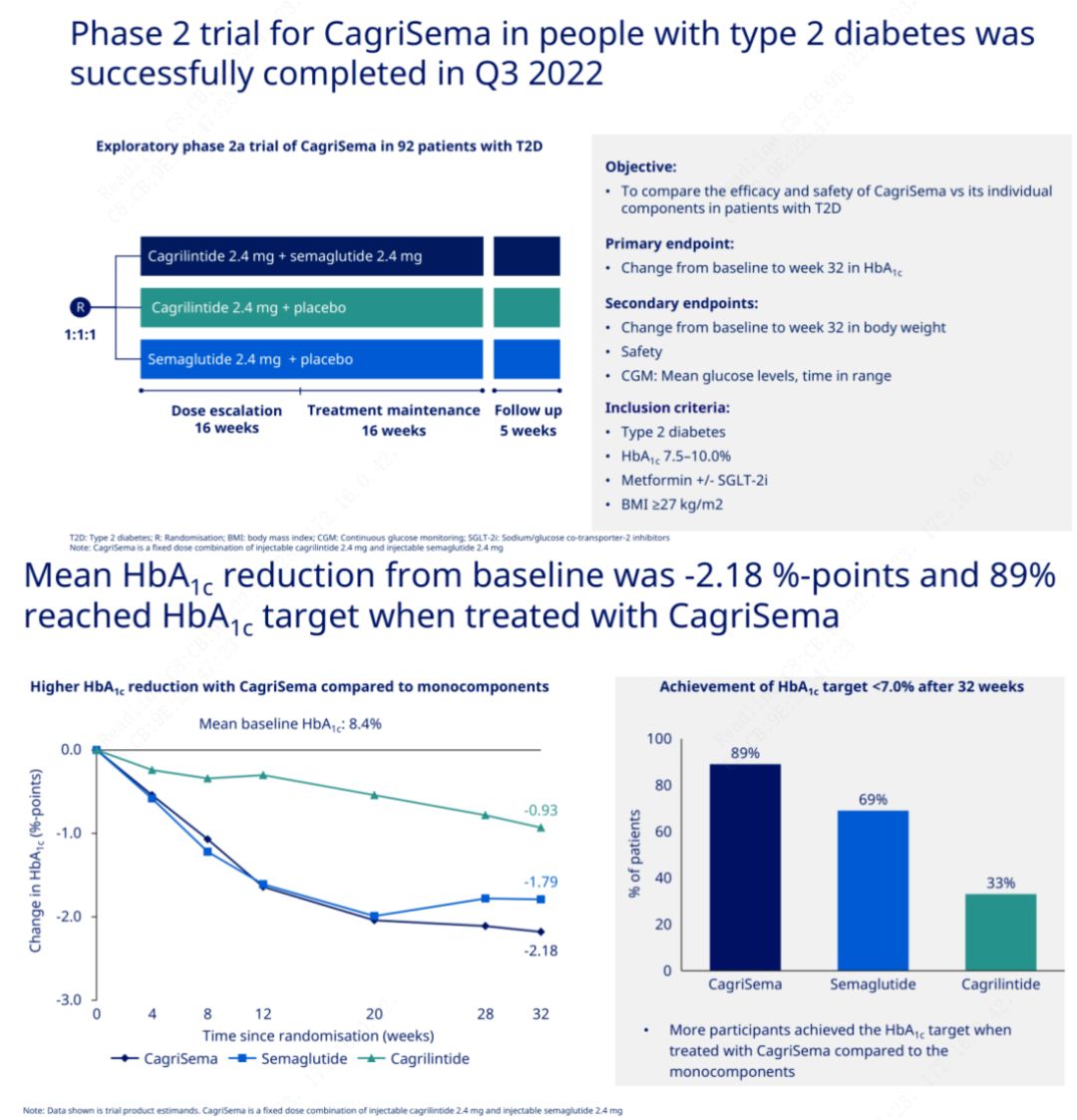
D'Daten weisen datt nieft dem bedeitende hypoglykemesche Effekt, a punkto Gewiichtsverloscht, d'CagriSema Injektioun däitlech besser wéi Semeglutid (5,1%) a Cagrilintide (8,1%) mat engem Gewiichtsverloscht vu 15,6% iwwerschratt huet.
Den innovativen Medikament Tirzepatide ass den éischten approuvéierte wöchentlechen GIP/GLP-1 Rezeptor Agonist op der Welt.Et kombinéiert d'Effekter vun zwee Inkretinen an eng eenzeg Molekül déi eemol d'Woch injizéiert gëtt an ass eng nei Klass vu Behandlungen fir Typ 2 Diabetis.Tirzepatide gouf vun der US Food and Drug Administration (FDA) am Mee 2022 guttgeheescht fir d'glykemesch Kontroll (op Diätbasis a Bewegung) bei Erwuessener mat Typ 2 Diabetis ze verbesseren an ass de Moment an der Europäescher Unioun, Japan an anere Länner guttgeheescht.
De 5. Juli huet d'Eli Lilly eng Phase III SURPASS-CN-MONO Studie ugekënnegt iwwer d'Medikamentklinesch Studieregistréierung an Informatiounsoffenbarungsplattform fir d'Behandlung vun Typ 2 Diabetis Patienten.SURPASS-CN-MONO ass eng randomiséierter, duebelblann, placebo-kontrolléiert Phase III Studie entwéckelt fir d'Effizienz a Sécherheet vun der Tirzepatid Monotherapie am Verglach zum Placebo bei Leit mat Typ 2 Diabetis ze evaluéieren.D'Etude huet geplangt 200 Patiente mat Typ 2 Diabetis opzehuelen, déi keng antidiabetesch Medikamenter an den 90 Deeg virum Besuch 1 hunn (ausser a bestëmmte klineschen Situatiounen, wéi akuter Krankheet, Hospitalisatioun oder elektive Chirurgie, kuerzfristeg (≤14) Deeg) Benotzung vun Insulin).
Typ 2 Diabetis gëtt erwaart dëst Joer guttgeheescht ze ginn
De leschte Mount goufen d'Resultater vun enger SURPASS-AP-Combo Studie de 25. Mee am Blockbuster Journal Nature Medicine publizéiert.D'Resultater weisen datt am Verglach mam Insulin glargin, Tirzepatide besser HbA1c a Gewiichtsreduktioun an der Bevëlkerung vun Typ 2 Diabetis Patienten an der Asien-Pazifik Regioun (haaptsächlech China) gewisen huet: HbA1c Reduktioun vu bis zu 2,49% a Gewiicht Reduktioun vu bis zu 7,2 kg (9,4%) op 40 Wochen Behandlung, bedeitend Verbesserung vun Blutt Lipiden a Blutdrock, an allgemeng Sécherheet an Toleranz waren gutt.
De Phase 3 klineschen Test vu SURPASS-AP-Combo ass déi éischt Studie vum Tirzepatide, haaptsächlech a chinesesche Patienten mat Typ 2 Diabetis duerchgefouert, gefouert vum Professer Ji Linong vum Peking University People's Hospital.SURPASS-AP-Combo ass konsequent mat de Resultater vun der globaler SURPASS Serie vu Fuerschung, déi weider beweist datt d'Pathophysiologie vun Diabetis bei chinesesche Patienten konsequent ass mat där vun globalen Patienten, wat d'Basis fir déi simultan Fuerschung an Entwécklung vun neien Drogen ass. a China an der Welt, a bitt och zolidd Beweiser Ënnerstëtzung fir Chinesesch Patienten d'Méiglechkeet ze ginn déi lescht Diabetisbehandlungsmedikamenter an hir klinesch Uwendung a China sou séier wéi méiglech ze benotzen.
Post Zäit: Sep-18-2023

